2月21日,国际学术期刊Nucleic Acids Research在线发表了中国科学院上海巴斯德研究所王建华研究员、武汉大学侯炜教授、北京协和医院李太生教授合作组的最新研究论文“Long noncoding RNA MALAT1 releases epigenetic silencing of HIV-1 replication by displacing the polycomb repressive complex 2 from binding to the LTR promoter”。该研究揭示长链非编码RNA (LncRNA) MALAT1诱使抑制性PRC2(polycomb repressive complex 2)复合物从HIV启动子LTR(长末端重复)解离从而促进HIV转录和复制。

近年来,长链非编码RNA(LncRNA)在表观遗传调控、免疫调节和细胞分化调控等方面的重要作用引起广泛关注。在调节HIV感染方面,通过靶向不同的细胞蛋白机器或信号通路,LncRNA可抑制或促进HIV复制。MALAT1主要定位于细胞核核斑(Nuclear speckles)区,可参与基因转录和pre-mRNAs的选择性剪接等细胞生理过程。 LncRNA MALAT1在肿瘤细胞中高表达,常被认为是肿瘤转移的标记物。
HIV高度依赖宿主因子完成复制周期,鉴定调节HIV复制的关键宿主因子可为抗病毒策略设计提供宿主新靶点。王建华研究组前期利用组学技术筛选了多种能够调控HIV复制的的宿主蛋白,如宿主蛋白SUN2通过维持HIV-LTR启动子区域异染色质结构抑制HIV转录和复制(2018,mBio);SAFB1通过抑制RNA聚合酶II的磷酸化并抑制其与HIV LTR的结合,抑制HIV的转录,维持HIV潜伏(2018,J.Bio.Chem);而宿主蛋白Naf1则是通过抑制NF-kB 信号通路抑制HIV复制(2016, J Virol)。
本研究中,王建华课题组联合武汉大学侯炜教授利用RNA-seq技术筛选出MALAT1在HIV感染细胞中高表达;高表达的MALAT1可促进HIV复制,CRISPR/Cas9敲除MALAT1可显著抑制HIV-LTR驱动的转录;机制上,MALAT1与PRC2抑制复合体中的组蛋白赖氨酸N-甲基转移酶EZH2(enhancer of zeste homolog 2)结合,使其从HIV-LTR上解离,减弱EZH2对HIV-LTR区核小体组蛋白的H3K27me3表观遗传学修饰(抑制性),使HIV-LTR维持在活跃状态,促进HIV转录;此外,与北京协和医院李太生教授合作,发现抗逆转录病毒药物治疗可显著降低HIV感染者外周血PBMC中MALAT1的表达,验证MALAT1表达与HIV复制的正相关性。该研究揭示LncRNA MALAT1调控HIV复制的重要作用和分子机制,即MALAT1诱使抑制性的PRC2复合物从HIV启动子LTR解离,通过减弱EZH2对HIV-LTR区核小体组蛋白的H3K27me3表观遗传学修饰,促进HIV转录和复制。为抗病毒策略设计提供了宿主新靶点。
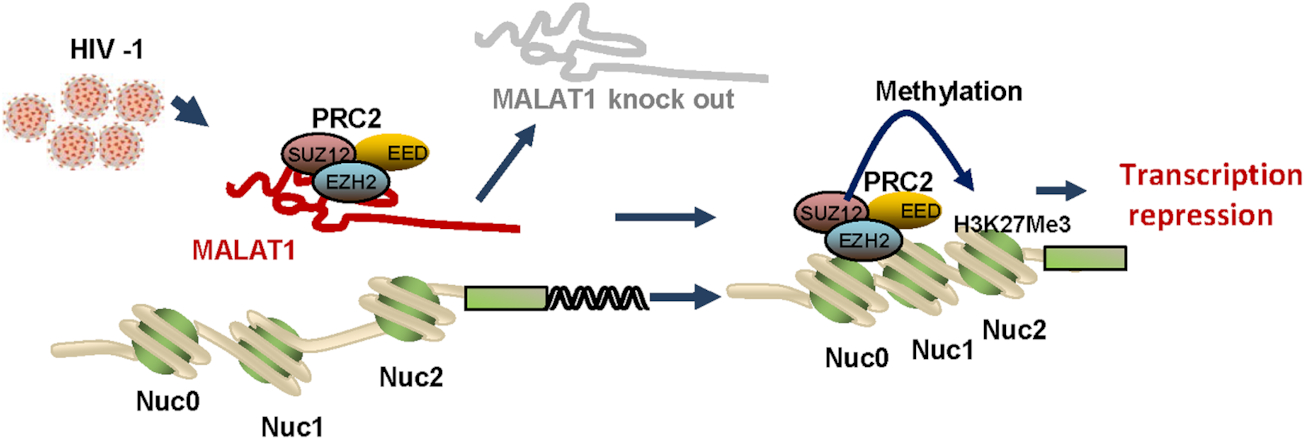
图1. MALAT1调节HIV复制的分子机制。
曲迪博士和孙玮玮博士为本文并列第一作者,王建华研究员、侯炜教授和李太生教授为并列通讯作者。该研究感谢上海巴斯德所金侠研究员的建议;该研究得到来自国家基金委、中科院及科技部艾滋病和病毒性肝炎重大传染病防治专项等项目的资助。
文章链接:
https://academic.oup.com/nar/advance-article/doi/10.1093/nar/gkz117/5351609
本文转载自“上海巴斯德研究所”
扩展阅读: